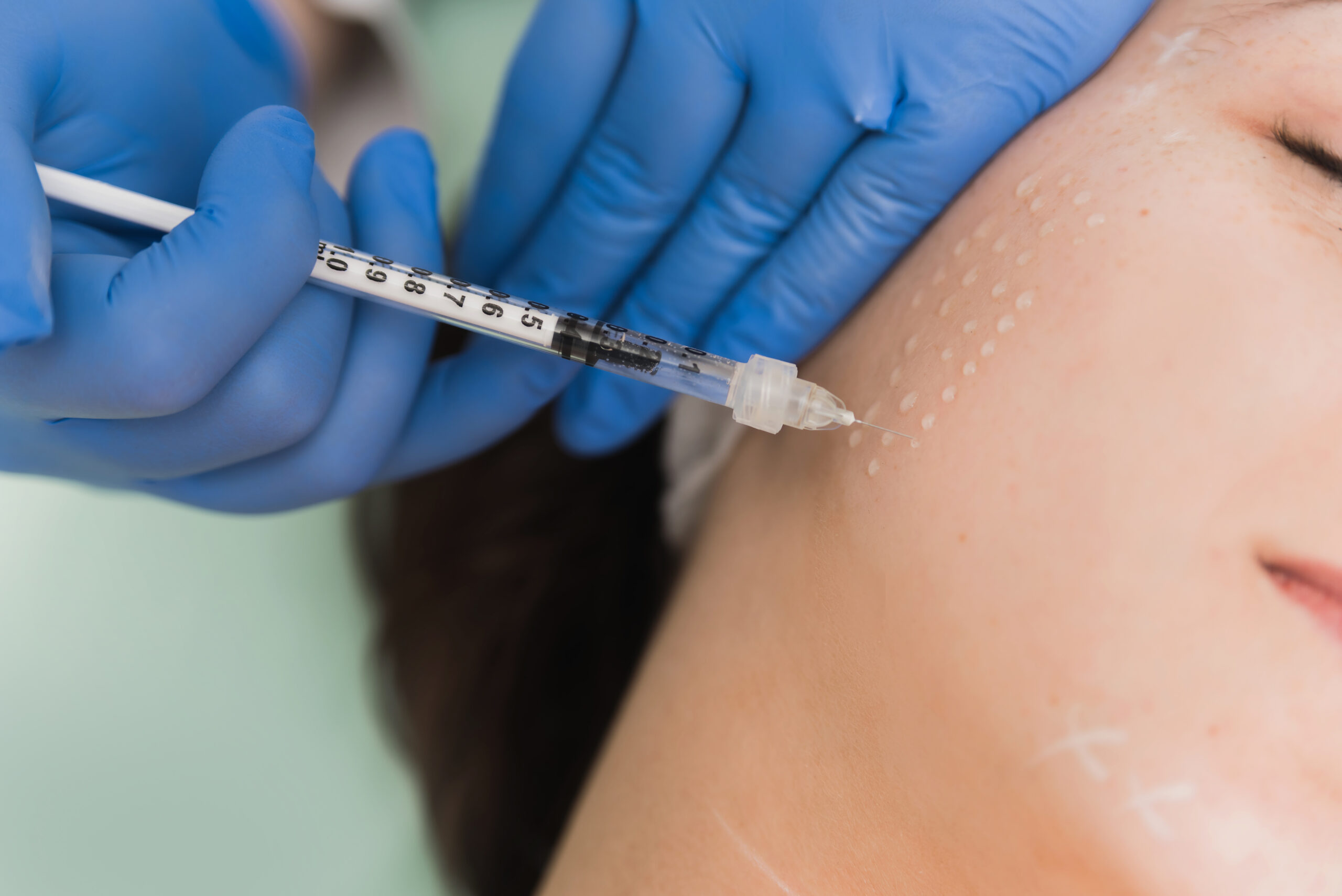
Połączenie kwasu hialuronowego i aminokwasów to jedna z najbardziej obiecujących strategii biorewitalizacji skóry w medycynie estetycznej. Jak działa na poziomie komórkowym, co mówią badania kliniczne i kiedy warto ją stosować w praktyce? Oto kompleksowe omówienie oparte na aktualnej wiedzy naukowej.

Prof. dr hab. n. med. Paweł Surowiak
Profesor Uniwersytetu Medycznego, współzałożyciel i były wieloletni członek zarządu oraz wiceprezes Polskiego Towarzystwa Medycyny Estetycznej i Anti-Aging. Autor licznych publikacji i podręczników, promotor bezpiecznej i opartej na dowodach praktyki medycznej. Współtwórca Dermamed Centrum Medycyny Estetycznej i Laseroterapii we Wrocławiu https://dermamed.com.pl
Znaczenie terapii poprawiających jakość skóry
W ostatnich latach w medycynie estetycznej rośnie znaczenie terapii ukierunkowanych na poprawę jakości skóry, rozumianej jako nawilżenie, elastyczność, jednorodność optyczna, gęstość echogeniczna skóry właściwej i subtelna poprawa mikrotekstury. Kwas hialuronowy jest tu kluczowy nie tylko jako klasyczny wypełniacz, lecz także jako składnik modyfikujący środowisko pozakomórkowe skóry. Kluczowy jest również fakt, że kwas hialuronowy wykazuje działanie przez specyficzne receptory, wpływając bezpośrednio na biologię komórek. Działanie to jest różne w zależności od wielkości cząsteczki kwasu hialuronowego.
Użycie mieszanek zawierających kwas hialuronowy i aminokwasy ma silne uzasadnienie biologiczne: hialuronian zapewnia nawilżenie i „matrycę” dla komórkowych procesów naprawczych, jest silnym stymulatorem, a aminokwasy (szczególnie glicyna, prolina i lizyna) dostarczają substratów do biosyntezy kolagenu i elastyny, wpływając zarazem na zachowanie fibroblastów. W praktyce przekłada się to na synergiczny bodziec do przebudowy macierzy zewnątrzkomórkowej i poprawy właściwości biomechanicznych skóry [1–3].
Mechanizmy działania: od „matrycy” do fibroblastu
Hialuronian jako główny glikozaminoglikan skóry utrzymuje uwodnienie i sprzyja dyfuzji czynników wzrostu, a przez interakcje z receptorami (m.in. CD44) moduluje migrację, przeżycie i aktywację fibroblastów. Różne rozmiary cząsteczek wywołują odmienne odpowiedzi: formy wysokocząsteczkowe sprzyjają homeostazie, a kontrolowane dawki fragmentów niskocząsteczkowych mogą inicjować krótkotrwały sygnał naprawczy i angiogenny, co w zabiegach iniekcyjnych jest wykorzystywane jako próba inicjacji procesów naprawczych.
Jednocześnie aminokwasy „kolagenowe” (glicyna, prolina i pochodne lizyny) przekładają się na realny potencjał biosyntetyczny fibroblastu, bo odpowiadają za ponad połowę składu aminokwasowego potrójnej helisy kolagenu i warunkują jej stabilność oraz sieciowanie [1–3].
Co pokazują modele in vitro?
Na ludzkich fibroblastach skóry wykazano, że połączenie kwasu hialuronowego z wybranym zestawem aminokwasów zwiększa żywotność komórek i wyraźnie podnosi ekspresję genów kolagenu typu I oraz elastyny (odpowiednio około 9,7-krotnie i 14-krotnie w przedziale 24–48 godzin), a także zwiększa o mniej więcej 15 proc. przeżywalność komórek. Są to zmiany, które dobrze tłumaczą późniejszą poprawę właściwości skóry mierzonych urządzeniami biomechanicznymi po serii iniekcji [4].
W innym doświadczeniu, z użyciem żelu zawierającego hialuronian oraz glicynę, prolinę, lizynę i leucynę, pobudzono proliferację fibroblastów oraz syntezę kolagenu typu I i III i fibronektyny, jednocześnie wzrosła ekspresja TGF-β i CTGF, czyli kluczowych mediatorów przebudowy macierzy [5].
Warto podkreślić, że skład ma znaczenie. W pilotażowym porównaniu popularnych koktajli mezoterapeutycznych nie wszystkie wieloskładnikowe mieszanki były korzystne: część zestawów bogatych w witaminy i mikroelementy obniżała przeżywalność fibroblastów, prowadząc do apoptozy i nekroza, podczas gdy roztwory oparte na hialuronianie z rozsądnie dobranymi komponentami utrzymywały proliferację i sprzyjały ekspresji kolagenu [6].
Dane kliniczne: co naprawdę dzieje się ze skórą po serii iniekcji?
W prospektywnym badaniu na 40 zdrowych dorosłych osobach, którym podawano kompleks hialuronianu uzupełniony aminokwasami i witaminami antyoksydacyjnymi w trzech sesjach co dwa tygodnie, odnotowano istotny statystycznie wzrost nawodnienia i poprawę właściwości sprężystych skóry mierzonych korneometrem i cutometrem. Procedura była dobrze tolerowana, bez poważnych działań niepożądanych [7].
W badaniu z oceną histologiczną i ultrasonograficzną, obejmującym iniekcje fragmentów niskocząsteczkowego hialuronianu połączonych z aminokwasami w skórę twarzy, wykazano w materiale biopsyjnym zwiększoną aktywność fibroblastów, wzrost liczby drobnych naczyń, pogrubienie naskórka oraz reorganizację włókien kolagenowych. Co ciekawe, pomiar grubości skóry w USG (w okolicy jarzmowej, brody, kąta żuchwy) nie uległ istotnej zmianie.
To zrozumiałe: we wczesnych fazach „remodelingu” zmienia się przede wszystkim jakość i mikroarchitektura tkanki, a nie jej grubość, dlatego w badaniach i praktyce warto preferować punkty końcowe w rodzaju gęstości echogenicznej, elasto-sonografii oraz panelu pomiarów biomechanicznych [8].
Dodatkowego kontekstu dostarcza praca z zastosowaniem nieusieciowanego hialuronianu bez dodatku aminokwasów: subdermalne podanie dwóch żeli nieusieciowanych skutkowało poprawą jakości skóry i pogrubieniem skóry właściwej w ultrasonografii po trzech tygodniach, przy dobrym profilu tolerancji. Wyniki te pokazują, że sam hialuronian może poprawiać parametry skin quality, a dodatek aminokwasów ma potencjał ukierunkować tę odpowiedź biologicznie (ECM, mikrokrążenie), co potwierdzają dane histologiczne i in vitro [9].
Praktyka: kiedy i jak stosować terapię HA + aminokwasy?
Pacjent idealny do terapii roztworami hialuronianu z aminokwasami to osoba z przesuszeniem, obniżoną elastycznością, drobnymi liniami i „zmęczonym” wyglądem skóry, bez dominujących ubytków objętości. Najczęściej stosowany, logiczny schemat to trzy sesje w odstępach dwutygodniowych z ewentualną sesją podtrzymującą po kilku miesiącach – właśnie w takich ramach uzyskiwano istotne poprawy pomiarów instrumentalnych.
Jeśli celem jest odbudowa wolumenu lub unoszenie tkanek, właściwym wyborem pozostaje usieciowany hialuronian o dobranych parametrach reologicznych, a roztwory HA + aminokwasy traktujemy jako program biorewitalizacji skóry.
Dla bezpieczeństwa i obiektywizacji efektów warto włączyć ultrasonografię wysokiej częstotliwości do planowania i monitorowania (mapowania przebiegu naczyń, kontroli depozytów, oceny gęstości echogenicznej skóry właściwej) [7, 9].
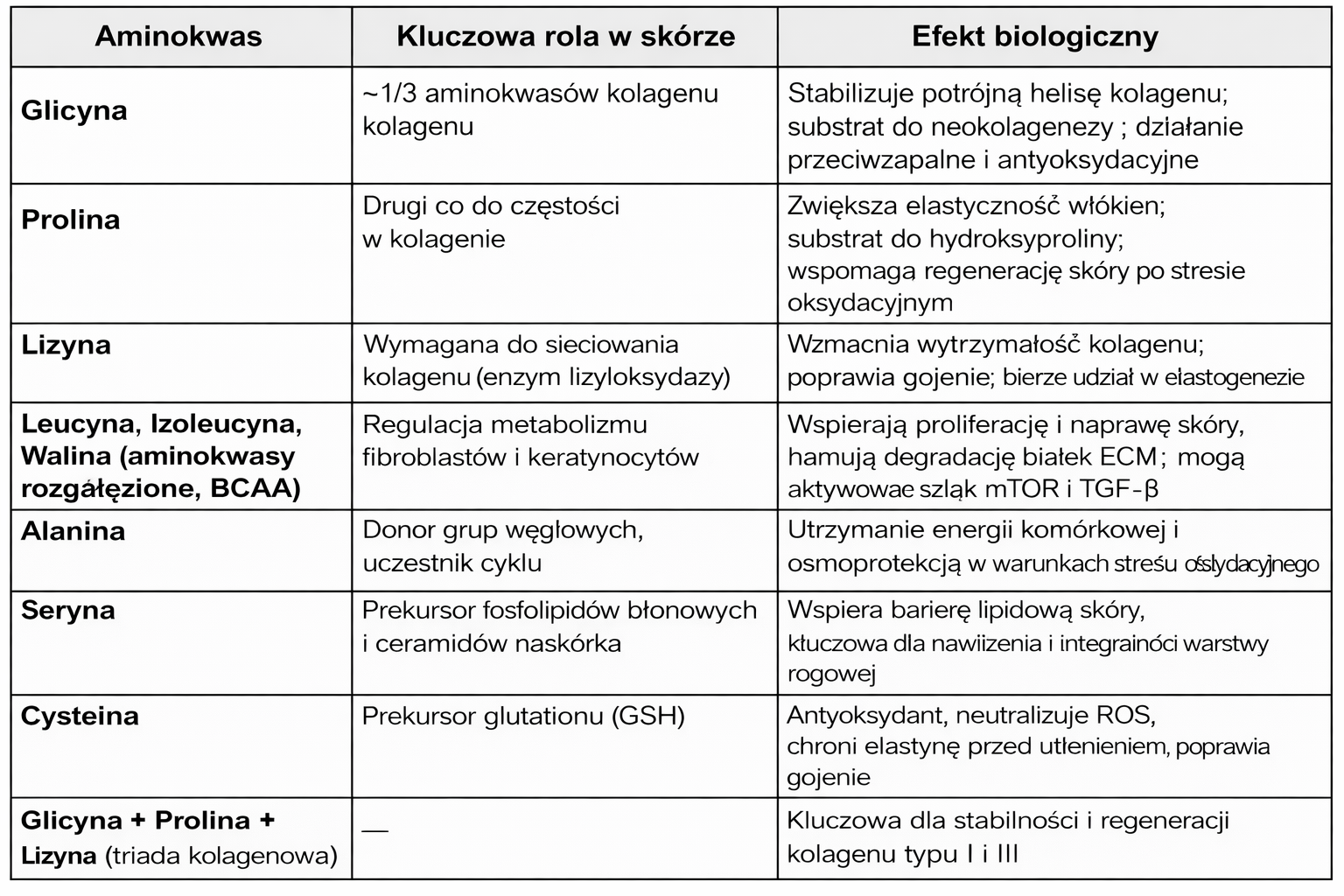
Mechanizmy działania w kontekście mezoterapii
izoleucyna, leucyna, lizyna, prolina, walina, glicyna, seryna, alanina, cysteina
1. Biostymulacja fibroblastów
- koktajle zawierające powyższą mieszankę (często z HA 1,0–1,5 proc.) aktywują fibroblasty przez zwiększenie ekspresji TGF-β1, COL1A1, FGF-2 i hamowanie MMP-1,
- badania in vitro pokazują, że leucyna i izoleucyna działają anabolicznie – zwiększają proliferację fibroblastów i syntezę kolagenu.
2. Ochrona antyoksydacyjna
- cysteina i glicyna są prekursorami glutationu, który neutralizuje ROS powstające pod wpływem UV i stresu oksydacyjnego,
- połączenie HA + cysteina skraca czas gojenia po peelingach i laseroterapii (Scarano 2023).
3. Synteza kolagenu i elastyny
- prolina i lizyna stanowią kluczowe aminokwasy w kolagenie, a niedobory tych aminokwasów ograniczają biosyntezę włókien ECM,
- w modelach skóry ludzkiej suplementacja tymi aminokwasami zwiększa ekspresję kolagenu I i III nawet bez bodźców zapalnych.
4. Regeneracja bariery naskórkowej
- seryna i alanina występują naturalnie w tzw. NMF (natural moisturizing factor). Wstrzyknięcie ich w głąb skóry śródskórnie może poprawiać hydratację i odbudowę warstwy rogowej.
5. Działanie synergiczne z kwasem hialuronowym
- HA zapewnia nawodnienie i środowisko sprzyjające proliferacji, z kolei aminokwasy stanowią substraty do syntezy kolagenu i elastyny – stąd efekt biorewitalizacji, nie tylko „wypełnienia”.
Bezpieczeństwo, jakość wyrobów i regulacje
Dostępne badania nad roztworami hialuronianu z aminokwasami i prace dotyczące nieusieciowanego HA wskazują na dobrą tolerancję: typowe objawy to krótkotrwały ból przy wkłuciu, niewielki obrzęk czy krwiaki. Ciężkie powikłania nie występowały w omawianych, niewielkich próbach.
Jednak standard kwalifikacji pacjenta, warunki jałowe i właściwa dokumentacja są kluczowe. Z perspektywy regulacyjnej warto pamiętać, że iniekcyjne preparaty hialuronianowe w Unii Europejskiej podlegają wymogom rozporządzenia MDR 2017/745 – z naciskiem na jakość wytwarzania, ocenę kliniczną i nadzór po wprowadzeniu do obrotu.
Obecne przeglądy wskazują na potrzebę jeszcze bardziej przejrzystego raportowania składu i właściwości reologicznych oraz na rosnącą rolę obiektywnych punktów końcowych w badaniach klinicznych [10–12].
Co dalej? Kierunki przyszłych badań
Kolejny krok to randomizowane badania kontrolowane porównujące roztwory hialuronianu z aminokwasami z samym hialuronianem, a także prace testujące proporcje poszczególnych aminokwasów pod kątem wpływu na ekspresję kolagenu i elastyny.
Należy standaryzować punkty końcowe: panel pomiarów biomechanicznych (np. cutometria), pomiary nawilżenia (korneometria), ultrasonografia wysokiej częstotliwości z analizą gęstości echogenicznej, a tam, gdzie to możliwe – potwierdzenia histologiczne (biomarkery ECM, barwienia włókien sprężystych).
Dopiero takie podejście pozwoli jednoznacznie zdefiniować miejsce HA + aminokwasów w algorytmach terapii jakości skóry.
Bibliografia
1. Chylińska N., Chrzanowski W., Bonifacio M.A., Hyaluronic Acid and Skin: Its Role in Aging and Wound Healing, „Gels” 2025, vol. 11(4), doi:10.3390/gels11040281.
2. Boraldi F., Schirosi L., Croce M.A., Tiozzo S., The Role of Fibroblasts in Skin Homeostasis and Repair, „International Journal of Molecular Sciences” 2024, vol. 25(7).
3. Tracy L.E., Minasian R.A., Caterson E.J., Extracellular Matrix and Dermal Fibroblast Function in the Healing Wound, „Advances in Wound Care” 2016, vol. 5(3).
4. Deglesne P.A. et al., In vitro study of RRS® HA injectable mesotherapy/biorevitalization product on human skin fibroblasts, „Clinical Cosmetic and Investigational Dermatology” 2016, vol. 9.
5. Mariggiò M.A. et al., Enhancement of fibroblast proliferation, collagen biosynthesis and growth factors induced by a pool of amino acids and sodium hyaluronate (Aminogam®), „Journal of Biological Regulators and Homeostatic Agents” 2009, vol. 22(2).
6. Jäger C., Brenner C., Habicht J., Wallich R., Bioactive reagents used in mesotherapy for skin rejuvenation in vivo induce diverse physiological processes in human skin fibroblasts in vitro – a pilot study, „Experimental Dermatology” 2012, vol. 21(1).
7. Siquier-Dameto G., Boadas-Vaello P., Verdú E., Intradermal Treatment with a Hyaluronic Acid Complex Supplemented with Amino Acids and Antioxidant Vitamins Improves Cutaneous Hydration and Viscoelasticity in Healthy Subjects, „Antioxidants” 2024, vol. 13(7), doi:10.3390/antiox13070770.
8. Scarano A. et al. The efficacy of hyaluronic acid fragments with amino acid in combating facial skin aging: an ultrasound and histological study, „Journal of Ultrasound” 2024. vol. 27.
9. Bezpalko L. et al., Clinical and Ultrasound Evaluation of Skin Quality After Superficial and Deep Injection of Two Non-Crosslinked Hyaluronic Acid Products, „Clinical, Cosmetic and Investigational Dermatology” 2023, vol. 16.
10. Allen J., Dodou K., Current Knowledge and Regulatory Framework on the Use of Hyaluronic Acid for Aesthetic Injectable Skin Rejuvenation Treatments, „Cosmetics” (MDPI) 2024, vol. 11(2).
11. Hong G.W. et al., Manufacturing Process of Hyaluronic Acid Dermal Fillers and Its Impact on Clinical Performance, „Polymers” (MDPI) 2024, vol. 16(19).
12. Jurczak K.M. et al., Recent regulatory developments in EU Medical Device field, „Bioengineering & Translational Medicine” 2024, vol. 9(6).